Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведенных в перечне, определите характер среды их водных растворов.
1) NaHCO3
2) MgI2
3) CsBr
4) HBr
Запишите номера веществ в порядке уменьшения значения рН их водных растворов, учитывая, что концентрация веществ во всех растворах (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведенных в перечне, определите характер среды их водных растворов.
1) Fe2(SO4)3
2) HClO3
3) KHCO3
4) Ca(NO3)2
Запишите номера веществ в порядке уменьшения значения pH их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Рассмотрим вещества из списка и их гидролиз:
1) Fe2(SO4)3 (Сульфат железа (III)). Соль слабого основания и сильной кислоты. Гидролизуется по катиону. Среда - слабокислая.
2) HClO3 (Хлорноватая кислота). Сильная кислота. Среда - сильнокислая.
3) KHCO3 (Гидрокарбонат калия). Соль сильного основания и слабой кислоты. Гидролизуется по аниону. Среда - слабощелочная.
4) Ca(NO3)2 (Нитрат кальция). Соль сильного основания и сильной кислоты. Не гидролизуется. Среда - нейтральная.
Распологаем вещества в порядке уменьшения (убывания) значения рН их водных растворов: KHCO3, Ca(NO3)2, Fe2(SO4)3, HClO3.
Переводим этот предварительный ответ в последовательность цифр, соответствующих веществам.
Ошибка.
Попробуйте повторить позже
В водном растворе метиламина среда раствора:
1) кислая
2) нейтральна
3) щелочная
4) слабокислая
Амины — производные аммиака, и их взаимодействие с водой протекает по аналогии с известной вам реакцией взаимодействия между аммиаком и водой:
CH3NH2 + H2O ⇆ CH3NH3+ + OH-
Среда водного раствора метиламина - щелочная
Ошибка.
Попробуйте повторить позже
Установите соответствие между названием соли и отношением ее к гидролизу.
| Название соли | Отношение к гидролизу |
| А) хлорид цинка | 1) гидролизуется по катиону |
| Б) сульфид калия | 2) гидролизуется по аниону |
| В) нитрат кальция | 3) гидролизуется по катиону и аниону |
| Г) нитрат меди (II) | 4) не гидролизуется |
Рассмотрим вещества из списка и их гидролиз:
А) хлорид цинка (ZnCl2) - соль слабого основания и сильной кислоты, следовательно, гидролизуется по катиону.
Б) сульфид калия (K2S) - соль сильного основания и слабой кислоты, следовательно, гидролизуется по аниону.
В) нитрат кальция (Ca(NO3)2) - соль сильного основания и сильной кислоты, следовательно, не гидролизуется.
Г) нитрат меди (II) (Cu(NO3)2) - соль слабого основания и сильной кислоты, следовательно, гидролизуется по катиону.
Соотнося буквы и цифры, получаем следующий предварительный ответ: А) - 1; Б) - 2; В) - 4; Г) - 1.
Переводим этот предварительный ответ в последовательность цифр, соответствующих отношениям к гидролизам.
Ошибка.
Попробуйте повторить позже
Установите соответствие между названием соли и отношением ее к гидролизу.
| Название соли | Отношение к гидролизу |
| А) нитрат калия | 1) гидролизуется по катиону |
| Б) сульфид бария | 2) гидролизуется по аниону |
| В) хлорид алюминия | 3) гидролизуется по катиону и аниону |
| Г) карбонат натрия | 4) не гидролизуется |
Рассмотрим вещества из списка и их гидролиз:
А) нитрат калия (KNO3) - соль сильного основания и сильной кислоты, следовательно, не гидролизуется.
Б) сульфид бария (BaS) - соль сильного основания и слабой кислоты, следовательно, гидролизуется по аниону.
В) хлорид алюминия (AlCl3) - соль слабого основания и сильной кислоты, следовательно, гидролизуется по катиону.
Г) карбонат натрия (Na2CO3) - соль сильного основания и слабой кислоты, следовательно, гидролизуется по аниону.
Соотнося буквы и цифры, получаем следующий предварительный ответ: А) - 4; Б) - 2; В) - 1; Г) - 2.
Переводим этот предварительный ответ в последовательность цифр, соответствующих отношениям к гидролизам.
Ошибка.
Попробуйте повторить позже
Установите соответствие между названием соли и ее отношением к гидролизу.
| Название соли | Отношение к гидролизу |
| А) хлорид калия | 1) гидролизуется по катиону |
| Б) фосфат натрия | 2) гидролизуется по аниону |
| В) сульфид магния | 3) гидролизуется по катиону и аниону |
| Г) нитрат алюминия | 4) не гидролизуется |
Рассмотрим вещества из списка и их гидролиз:
А) хлорид калия (KCl) - соль сильного основания и сильной кислоты, следовательно, не гидролизуется.
Б) фосфат натрия (Na3PO4) - соль сильного основания и слабой кислоты, следовательно, гидролизуется по аниону.
В) сульфид магния (MgS) - соль слабого основания и слабой кислоты, следовательно, гидролизуется и по катиону, и по аниону.
Г) нитрат алюминия (Al(NO3)) - соль слабого основания и сильной кислоты, следовательно, гидролизуется по катиону.
Соотнося буквы и цифры, получаем следующий предварительный ответ: А) - 4; Б) - 2; В) - 3; Г) - 1.
Переводим этот предварительный ответ в последовательность цифр, соответствующих отношениям к гидролизам.
Ошибка.
Попробуйте повторить позже
Установите соответствие между формулой соли и отношением этой соли к гидролизу.
| Формула соли | Отношение к гидролизу |
| А) KNO3 | 1) гидролизуется по катиону |
| Б) CuF2 | 2) гидролизуется по аниону |
| В) CrBr3 | 3) гидролизуется по катиону и аниону |
| Г) CH3COOK | 4) не гидролизуется |
Рассмотрим вещества из списка и их гидролиз:
А) KNO3 - соль сильного основания и сильной кислоты, следовательно, не гидролизуется.
Б) CuF2 - соль слабого основания и слабой кислоты, следовательно, гидролизуется и по катиону, и по аниону.
В) CrBr3 - соль слабого основания и сильной кислоты, следовательно, гидролизуется по катиону.
Г) CH3COOK - соль сильного основания и слабой кислоты, следовательно, гидролизуется по аниону.
Соотнося буквы и цифры, получаем следующий предварительный ответ: А) - 4; Б) - 3; В) - 1; Г) - 2.
Переводим этот предварительный ответ в последовательность цифр, соответствующих отношениям к гидролизам.
Ошибка.
Попробуйте повторить позже
Одинаковую реакцию среды имеют растворы хлорида калия и
1) нитрата алюминия
2) хлорида цинка
3) сульфата железа (II)
4) нитрата натрия
5) бромата калия
"Одинаковую реакцию среды имеют растворы хлорида калия и..."
Чтобы решить задачу, нужно определить среду раствора хлорида калия и определить растворы каких веществ имеют такую же среду.
"Реакцию среды" можно "грубо" перефразировать как "среду", для лучшего понимания.
Определим среду раствора хлорида калия:
Хлорид калия (KCl) - соль сильного основания и сильной кислоты. Не гидролизуется. Среда его раствора - нейтральная.
Проанализируем среды растворов веществ из списка и найдем те, которые нам нужны - растворы с нейтральной средой.
1) Нитрат алюминия (Al(NO3)3) - соль слабого основания и сильной кислоты. Гидролизуется по катиону. Среда его раствора - слабокислая. Не подходит.
2) Хлорид цинка (ZnCl2) - соль слабого основания и сильной кислоты. Гидролизуется по катиону. Среда его раствора - слабокислая. Не подходит.
3) Сульфат железа (II) (FeSO4) - соль слабого основания и сильной кислоты. Гидролизуется по катиону. Среда его раствора - слабокислая. Не подходит.
4) Нитрат натрия (NaNO3) - соль сильного основания и сильной кислоты. Не гидролизуется. Среда его раствора - нейтральная. Подходит.
5) Бромат калия (KBrO3) - соль сильного основания и сильной кислоты. Не гидролизуется. Среда его раствора - нейтральная. Подходит.
Мы нашли нужные растворы веществ. Переводим этот предварительный ответ в последовательность цифр, соответствующих веществам.
Ошибка.
Попробуйте повторить позже
Наибольшее количество нитрат-ионов образуется в растворе
при диссоциации 1 моль
1) нитрата алюминия
2) нитрата меди (II)
3) нитрата натрия
4) нитрата кальция
5) нитрата железа (III)
Напишем уравнения диссоциации веществ и проанализируем их по количеству нитрат-ионов:
1) Al(NO3)3 ⇔ Al3+ + 3 NO3-. Из 1 моля соли образуется 1 моль ионов алюминия и 3 моля нитрат-ионов. Количество каждой соли - 1 моль, коэффициент перед ними равен 1 (хоть он и не прописан). Следовательно, на каждую единицу коэффициента приходится 1 моль ионов. Коэффициент у нитрат-ионов равен 3, значит и их 3 моль. По такой логике определим количество остальных ионов.
2) Cu(NO3)2 ⇔ Cu2+ + 2 NO3-. Из 1 моля соли образуется 1 моль ионов меди и 2 моля нитрат-ионов.
3) NaNO3 ⇔ Na+ + NO3-. Из 1 моля соли образуется 1 моль ионов натрия и 1 моль нитрат-ионов.
4) Ca(NO3)2 ⇔ Ca2+ + 2 NO3-. Из 1 моля соли образуется 1 моль ионов кальция и 2 моля нитрат-ионов.
5) Fe(NO3)3 ⇔ Fe3+ + 3 NO3-. Из 1 моля соли образуется 1 моль ионов железа и 3 моля нитрат-ионов.
Наибольшее число выделяемых нитрат-ионов равно 3 моль. Ищем вещества, которые при диссоциации могут выделить 3 моля нитрат-ионов. Это нитрат железа (III) и нитрат алюминия.
Переводим этот предварительный ответ в последовательность цифр, соответствующих веществам.
Ошибка.
Попробуйте повторить позже
Нейтральную среду имеют водные растворы
1) нитрата калия
2) силиката натрия
3) сульфата лития
4) нитрита калия
5) хлорида железа (II)
Рассмотрим вещества из списка и среду их растворов:
1) Нитрат калия (KNO3) - соль сильного основания и сильной кислоты. Не гидролизуется. Среда раствора этого вещества - нейтральная. Подходит
2) Силикат натрия (Na2SiO3) - соль сильного основания и слабой кислоты. Гидролизуется по аниону. Среда раствора этого вещества - слабощелочная. Не подходит.
3) Сульфата лития (Li2SO4) - соль сильного основания и сильной кислоты. Не гидролизуется. Среда раствора этого вещества - нейтральная. Подходит.
4) Нитрита калия (KNO2) - соль сильного основания и слабой кислоты. Гидролизуется по аниону. Среда раствора этого вещества - слабощелочная. Не подходит.
5) Хлорида железа (II) (FeCl2) - соль слабого основания и сильной кислоты. Гидролизуется по катиону. Среда раствора этого вещества - слабокислая. Не подходит.
Переводим этот предварительный ответ в последовательность цифр, соответствующих веществам.
Ошибка.
Попробуйте повторить позже
Одинаковую реакцию среды имеют растворы карбоната натрия и
1) нитрата бария
2) силиката калия
3) фосфата натрия
4) сульфата цинка
5) хлорида алюминия
"Одинаковую реакцию среды имеют растворы карбоната натрия и..."
Чтобы решить задачу, нужно определить среду раствора карбоната натрия и определить растворы каких веществ имеют такую же среду.
"Реакцию среды" можно "грубо" перефразировать как "среду", для лучшего понимания.
Определим среду раствора карбоната натрия:
Карбонат натрия (Na2CO3) - соль сильного основания и слабой кислоты. Гидролизуется по аниону. Среда - слабощелочная.
Проанализируем среды растворов веществ из списка и найдем те, которые нам нужны - растворы с слабощелочной средой.
1) Нитрат бария (Ba(NO3)2) - соль сильного основания и сильной кислоты. Не гидролизуется. Его раствор имеет нейтральную среду. Не подходит.
2) Силикат калия (K2SiO3) - соль сильного основания и слабой кислоты. Гидролизуется по аниону. Его раствор имеет слабощелочную среду. Подходит.
3) Фосфат натрия (Na3PO4) - соль сильного основания и слабой кислоты. Гидролизуется по аниону. Его раствор имеет слабощелочную среду. Подходит.
4) Сульфат цинка (ZnSO4) - соль слабого основания и сильной кислоты. Гидролизуется по катиону. Его раствор имеет слабокислую среду. Не подходит.
5) Хлорида алюминия (AlCl3) - соль слабого основания и сильной кислоты. Гидролизуется по катиону. Его раствор имеет слабокислую среду. Не подходит.
Мы нашли нужные растворы веществ. Переводим этот предварительный ответ в последовательность цифр, соответствующих веществам.
Ошибка.
Попробуйте повторить позже
Диссоциация ортофосфорной кислоты по второй ступени происходит в соответствии с уравнением
1) HPO42- ⇆ H+ + PO43-
2) H3PO4 ⇆ H+ + H2PO4-
3) H2PO4- ⇆ H+ + HPO42-
4) H3PO4 ⇆ 3H+ + PO43-
Диссоциация ортофосфорной кислоты проходит по трем ступеням:
1) H3PO4 ⇆ H+ + H2PO4-
2) H2PO4- ⇆ H+ + HPO42-
3) HPO42- ⇆ H+ + PO43-
Следовательно, диссоциация по второй ступени проходит в соответствии с уравнением:
H2PO4- ⇆ H+ + HPO42-
Таким образом, нам подходит цифра 3.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
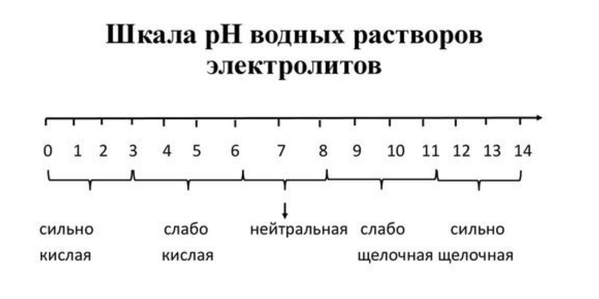
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) LiBr
2) HI
3) KF
4) FeSO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация веществ во всех растворах (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Cr(NO3)2
2) Ca(OH)2
3) CH3COONH4
4) HClO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4NO3
2) CH3COOK
3) BaCl2
4) RbOH
Запишите номера веществ в порядке возрастаия значения pH их водных растворов, учитывая. что концентрация всех растворов (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaClO3
2) KClO
3) (NH4)2SO4
4) HI
Запишите номера веществ в порядке убывания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите, характер сред их водных растворов.
1) Al(NO3)3
2) NH3
3) CH3COONH4
4) HClO3
Запишите номера веществ в порядке возрастания значения pH их вдных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HCOOH
2) CH3COOK
3) Sr(OH)2
4) KI
Запишите номера веществ в порядке убывания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
1) HCOOH - кислота, среда кислая.
2) CH3COOK - соль сильного основания и слабой кислоты, подвергается гидролизу по аниону, среда слабощелочная.
3) Sr(OH)2 - сильное основание, среда сильнощелочная.
4) KI - соль сильного основания и сильной кислоты, гидролизу не подвергается, среда нейтральная.
Распологаем вещества в порядке убывания значения рН их водных растворов: Sr(OH)2, CH3COOK, KI, HCOOH.
Переводим этот предварительный ответ в последовательность цифр, соответствующих веществам.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2S
2) NaNO2
3) Ca(NO3)2
4) HBr
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Ошибка.
Попробуйте повторить позже
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H3PO4
2) Na3PO4
3) NaNO3
4) Ba(OH)2
Запишите номера веществ в порядке возрастания значения pH их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.



